Een doorbraak: voor het eerst komt er een medicijn op de markt dat de ziekte van Alzheimer bij de oorzaak aanpakt. Wat betekent dat voor Nederlandse patiënten en waarom is nog niet iedereen enthousiast?
Het medicijn Aducanumab is door de Amerikaanse toezichthouder van gezondheidszorg (de FDA) goedgekeurd. Het mag dus op de Amerikaanse markt worden voorgeschreven door artsen.
Om op dit punt te komen deden wereldwijd 3.300 mee aan de tests van dit medicijn, waaronder 34 Nederlanders. Deze 34 Nederlanders met milde cognitieve stoornissen (MCI) of het beginstadium van de ziekte van Alzheimer namen deel aan het onderzoek bij onze partner, het Nederlandse Brain Research Center.
Wat doet het medicijn?
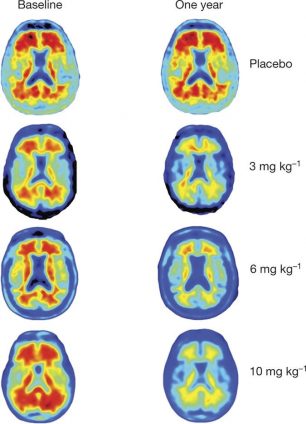
Het kan bij een deel van de mensen met beginnende alzheimer het ziekteproces licht vertragen. Het middel zorgt ervoor dat het schadelijke Alzheimer-eiwit amyloid wordt weggeruimd uit de hersenen. Het medicijn spoelt als het ware de hersenen schoon. Je kunt dat zien op de afbeelding hier rechts.
Bovenaan de afbeelding zie je hersenen van mensen die een placebo kregen, een nepmedicijn. Links zijn de hersenen voor de behandeling. Rechts zijn de hersenen na een jaar behandeling. De rode kleur duidt op een hoge amyloid concentratie.
De hersenen daaronder zijn van mensen die Aducanumab kregen, in verschillende hoeveelheden. Na een jaar behandeling is de concentratie amyloid sterk afgenomen. Hoe hoger de dosis, hoe meer amyloid werd verwijderd uit het brein.
Beluister de podcast waarin de directeur van het Brain Research Center uitlegt hoe het medicijn werkt.
Waarom is nog niet iedereen dolenthousiast?
Hoewel het medicijn duidelijk effectief is in het aanpakken van één van de bronnen van de ziekte (het wegruimen van het amyloid eiwit), zien we nog niet heel duidelijk in deze studies dat mensen met de ziekte door het medicijn minder snel achteruit gaan. Het kan bij een deel van de mensen met beginnende alzheimer het ziekteproces licht vertragen. De wetenschap zegt dan dat er geen overduidelijk ‘klinisch effect’ is. Biologisch wel.
Bekijk hier hoe Alzheimer Nederland veel gestelde vragen beantwoordt.
Professor Philip Scheltens, neuroloog en directeur van Alzheimercentrum Amsterdam, reageert hier in het programma Op1 als volgt op: “Als we een kankertumor met een behandeling kunnen verkleinen, maar de patiënt of de dokter merkt dat niet meteen, moet je het dan niet toedienen? Ik weet zeker dat veel patiënten zullen zeggen ‘Als ik ervoor kan zorgen dat ik met een behandeling de ziekte in mijn hersenen tot stilstand kan brengen, geef die behandeling dan maar. Ook als ik in de eerste paar jaar de effecten niet direct ervaar’. Er moet inderdaad nog meer onderzoek plaatsvinden om ook de klinische effecten verder aan te tonen.”
Bekijk hieronder het webinar dat prof. Philip Scheltens gad over het nieuws rond dit nieuwe medicijn.
Wat betekent dit voor Nederlanse patiënten?
Het is nog niet de oplossing voor iedere patiënt met de ziekte van Alzheimer. Slechts een kleine groep patiënten komt voor dit middel in aanmerking. De Amerikaanse goedkeuring geeft een belangrijk signaal dat het daadwerkelijk mogelijk is om iets te doen aan de hersenschade die ontstaat door alzheimer.
Nu buigt de Europese medicijn autoriteit (EMA) zich over dezelfde resultaten. Als zij het medicijn ook goedkeuren kan het ook in Nederland op de markt komen. De betrokken instanties bereiden zich nu al voor om het Nederlandse zorgsysteem klaar te maken. Ze verwachten dat de EMA eind 2021 een uitspraak zal doen. Er wordt dan bepaald wie in aanmerking komt voor het middel, hoeveel het het gaat kosten en wat de procedure wordt als artsen het mogen voorschrijven.
Bekijk het webinar
Op 7 juni kwam het nieuws naar buiten. Op 10 juni gaf Prof. dr. Philip Scheltens deze toelichting:
Bekijk de reactie van een van de deelnemers die het middel krijgt en anderen wetenschappers in het Alzheimerveld